まず、molについて。
化学基礎の最初の方でやりましたが、この世の中を物質を構成する粒子である原子は0.1nmぐらいと、めっちゃ小さいので、扱いにくいんですよ。
そこで、粒子を6.0×10²³(アボガドロ定数)個集めたものを1molとしました。(鉛筆12本を1ダースと呼ぶのと同じノリです。)(こうすることで肉眼で見えるくらいになります。)
つまりmolって言わば個数のことなんですよね。だから、個数で言える関係はmolでも同じ関係が成り立ちます。
ていうのを踏まえた上で、、、
3の5(7)
塩化マグネシウムは化学式ではMgCl₂と表されます。
つまり、MgCl₂「1個」はMg²⁺が「1個」、Cl⁻が2個でできています。
ということは、MgCl₂が「1mol」なら、Mg²⁺は「1mol」、Cl⁻は「2mol」となります。
で、今回はMgCl₂が0.20molなので、Cl⁻は「0.40mol」となります。
したがって、図の関係を使うと、0.40×6.0×10²³をすれば答えが出ます。
質問で、図の関係が使えないのか?ときいていましたが、もし、0.20×6.0×10²³としてしまうと、0.20というのは「MgCl₂」のmolなので、「MgCl₂」の個数が出てきます。
ただ、今回求めたいのは、「Cl⁻」の個数なので、「Cl⁻」のmolにアボガドロ定数を掛けないといけないです。
同様にして考えると、
3の7
(5)C₂H₄が1個で、Hが4個なので、水素の個数を4分の1倍することで、エチレンの個数が出ます。
で、それをアボガドロ定数で割ることで、molが出て、22.4倍することで体積が出ます。
(6)「質量で何パーセントか」→「酸素のg÷二酸化炭素のg」ということです。
で、gを出すためにはmolが必要なのですが、わからないので、CO₂のmolをx(mol)としてみましょうか。
CO₂が1個でCが1個、Oが2個ということなので、CO₂がx(mol)でCがx(mol)、Oが2x(mol)ということです。
よって、「(2x×酸素の原子量)÷(x×二酸化炭素の分子量)」で答えが出ます。
(7)これは普通に図の通りに計算するだけですよ。
「1÷アボガドロ定数」で水のmolが出て、それに分子量をかけることで答えがでます。
(8)こういうタイプの問題は求めたいものを文字で置いてみましょう。
というわけで、求める原子量をxと置いてみましょう。すると、、、
「質量が4.5×10²³、原子量がx」→「(4.5×10²³)÷x」でmolが出て、
「原子1個」→「1÷アボガドロ定数」でmolが出る
ってことで、2つとも同じmol数なので、方程式ができて、あとはそれを解くだけです。




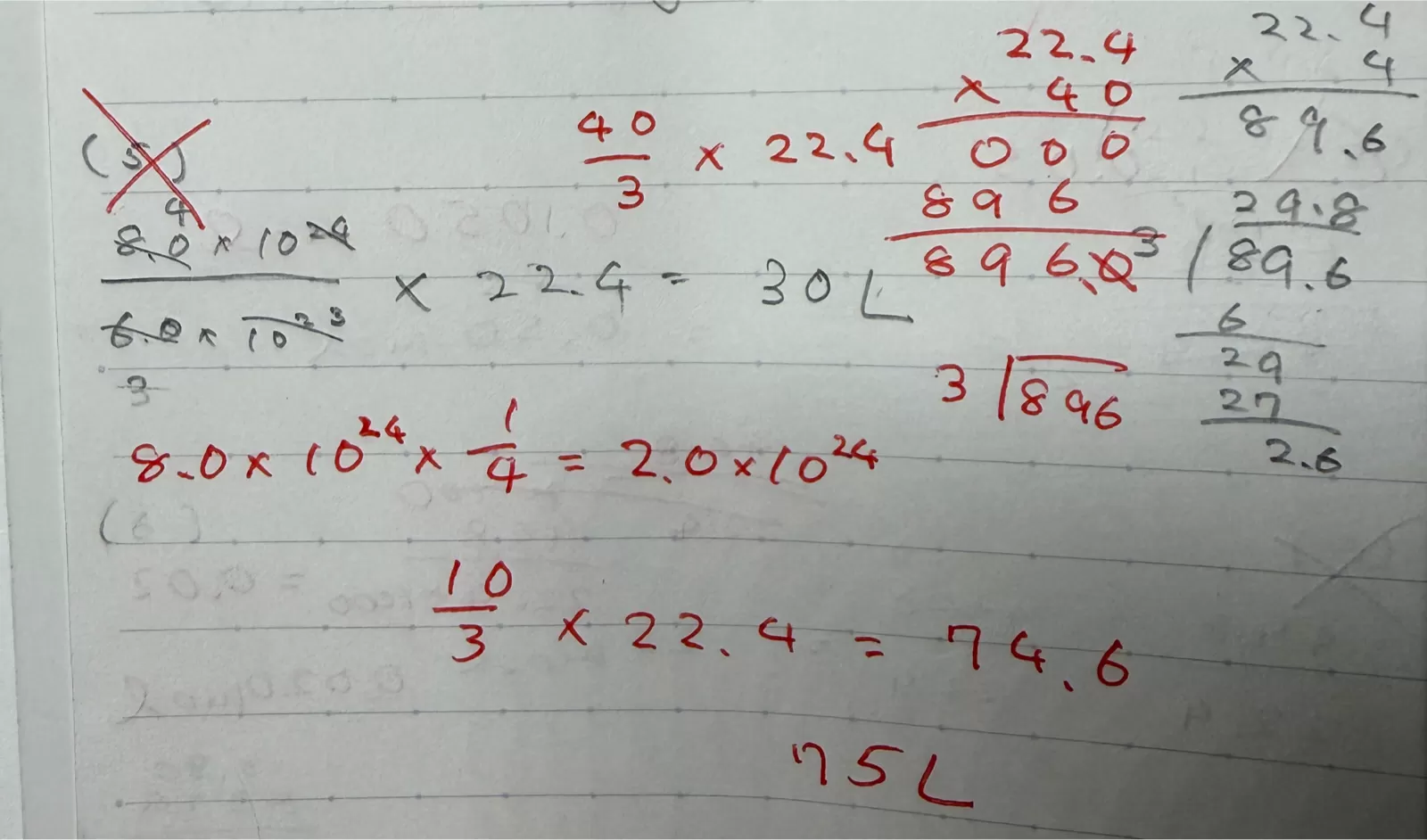














この通りにしても解けなかったです、!